“比特派钱包下载网址让我在加密货币世界中游刃有余。交易速度超快,手续费超低。无论是管理多种加密资产还是参与智能合约项目,都是绝佳选择。”
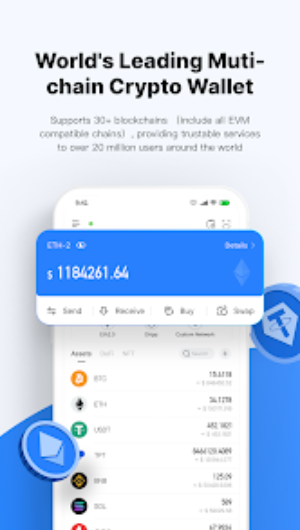
比特派钱包下载网址
比特派钱包下载网址是一款支持多链的自托管钱包,使用简单安全,深受全球数千万人的信赖与喜爱
我们的应用费率
为您制定定价计划
反馈
人们在谈论什么.
发现
常见问题
区块链是一个共享数据库,存储于其中的数据或信息,具有不可伪造、全程留痕、可以追溯、公开透明和集体维护等特征。可以把区块链理解为一个共享的、不可更改的电子账本,能够在网络中记录交易和跟踪资产。这里的资产可以是有形的(例如房和车),也可以是无形的(例如知识产权、专利和品牌)。几乎任何有价值的东西都可以在区块链网络上进行跟踪和交易,从而降低各方面的风险和成本。 目前区块链技术最大的应用是数字货币,因为支付的本质是“将账户A中减少的金额增加到账户B中”。如果人们有一本公共账簿,记录了所有的账户至今为止的所有交易,那么对于任何一个账户,人们都可以计算出它当前拥有的金额数量。而区块链恰恰是用于实现这个目的的公共账簿,其保存了全部交易记录。 区块链起源于比特币,2008年11月1日,一位自称中本聪(Satoshi Nakamoto)的人发表了《比特币:一种点对点的电子现金系统》一文,阐述了基于P2P网络技术、加密技术、时间戳技术、区块链技术等的电子现金系统的构架理念,这标志着比特币的诞生。两个月后理论步入实践,2009年1月3日第一个序号为0的创世区块诞生。几天后2009年1月9日出现序号为1的区块,并与序号为0的创世区块相连接形成了链,标志着区块链的诞生。
【安卓版本】 安卓手机用户请到比特派钱包下载网址官网下载最新版本。 (注意:比特派钱包下载网址官方网址为:https://www.monit8021.com) 【苹果版本】 点击下方链接查看苹果手机如何在App Store下载比特派钱包下载网址 App?https://www.monit8021.com
相对于私钥掌握在第三方服务商手中的中心化钱包(交易所),去中心化钱包的私钥则由用户自己保存,资产存储在区块链上,用户是真正的数字货币的持有者,钱包只是帮助用户管理链上资产和读取区块链数据的一个工具,所以也就无法控制、窃取、转移你的资产。 因此去中心化的钱包很难被黑客集中攻击,用户也不必担心钱包服务商的自我窃取或者跑路,因为只要创建钱包的时候自己把私钥保管好,您的资产依然在链上,换个钱包一样可以显示出来的。 注意:去中心化钱包一旦丢失、被盗,在没有备份私钥或助记词的情况下是无法找回的,因此一定要安全、正确的备份您的私钥。
矿工费(Gas Fee)也称为网络费,顾名思义就是支付给矿工的手续费,当您在区块链上进行转账时,矿工(或节点)需要把您的转账交易打包并放上区块链,才能使交易完成,在这过程中会消耗区块链的运算资源,因此产生矿工费用。 在EVM兼容链中,手续费是由Gas Price(单价)和消耗的 Gas Limit(数量)来确定的,其中计算公式如下: 矿工费 = Gas Limit * Gas Price Gas Limit数量主要受根据智能合约的内容操作复杂程度影响。操作越多,Gas limit越高。Gas Price是由发起方设置的,发起方设置的Gas Price的价格越高,其发起的交易就能越快被打包。 注: 以太坊(Ethereum)的网络费为ETH; 币安智能链(BNBChain)的网络费为BNB; 波场(TRON)的网络费为TRX; 马蹄(Polygon/Matic)的网络费为MATIC; Solana的网络费为SOL; OKExChain的网络费为OKT; 网络用不完是可以退回的。 转账网络收取的矿工费(网络费)会根据网络的情况而有所不同,一旦确定交易,不管交易是否成功,矿工费都无法退回。 矿工费是由您所选取的转账网络进行收取,比特派钱包下载网址钱包不收取任何费用!
DeFi全称为Decentralized Finance,即“去中心化金融”或者“分布式金融”。它与传统中心化金融相对,指建立在开放的去中心化网络中的各类金融领域的应用,用户无需再在中心化机构的辅助下参与金融市场,而是可以利用去中心化网络中的开源软件获得、交易并借贷资产。通俗的说,就是建立一个对所有人开放的新金融系统,不需要如银行这类的中介机构。 DeFi的目标是建立一个多层面的金融系统,以区块链技术和密码货币为基础,重新创造并完善已有的金融体系。 当前,几乎全部的DeFi项目都在以太坊的区块链上进行,智能合约是 DeFi的主要构建模块。如今最常见的几类 DeFi Dapp主要有Compound、MakerDAO、Synthetix、去中心化交易所(例如Uniswap)等。
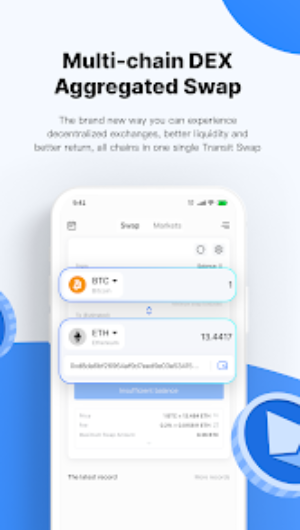
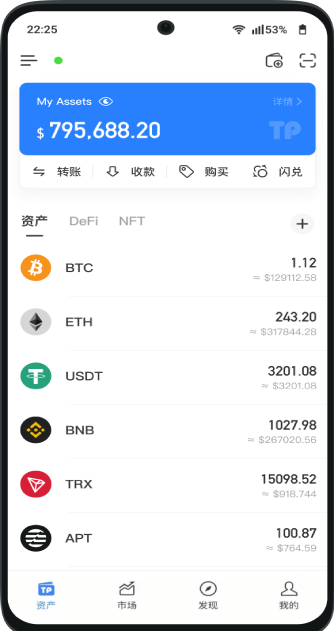
界面
看看应用程序里面有什么
比特派钱包下载网址官网Android 和 iOS 下载
3 00 万用户并且还在增加!
专注与比特派钱包下载网址相关报道,区块链行业动态,加密货币百科技术
最近的新闻
数字货币跟单操作指南:从入门到精通
什么是数字货币跟单操作? 数字货币跟单操作是指投资者通过某个跟单平台,将自己的交易账户与一位经验丰富、收益稳定的优秀交易者账户进行绑定,在该交易者进行交易操作时,自动跟随其交易策略进行相同的交易,实现收益共享。 如何选择适合的数字货币跟单平台? 在选择数字货币跟单平台时,需要考虑以下因素:平台的可信度和安全性、平台提供的跟单交易者的胜率和收益率、平台...
6个替代数字货币支付的方式
1. 现金支付 在数字货币出现之前,现金支付是人们最常用的支付方式之一。现金支付简单方便,不需要任何技术设备,而且对于一些特殊场合或交易,使用现金支付更为合适。 2. 银行卡支付 银行卡支付是目前广泛使用的支付方式之一。通过使用借记卡或信用卡,用户可以直接从自己的银行账户中扣款进行支付。银行卡支付具有便利性和安全性,并且被广泛接受。 3. 支付宝/...
如何解决TP钱包显示余额不足的问题
为什么我的TP钱包会显示余额不足? 您的TP钱包显示余额不足,可能是由于以下原因导致的: 您的TP钱包余额确实不足,可能是在之前的交易中消耗了大部分余额。 您的TP钱包正在同步区块链,还未完全同步完成,因此出现余额不足的提醒。 您的TP钱包可能被黑客攻击或遭受诈骗,导致资金被盗。 如何解决TP钱包显示余额不足的问题? 要解决TP钱包显...